Danas je nealkoholna masna bolest jetre (NAFLD) postala glavni uzrok kronične bolesti jetre u Kini, pa čak i u svijetu. Spektar bolesti uključuje jednostavni hepatički steatohepatitis, nealkoholni steatohepatitis (NASH) i srodnu cirozu i rak jetre. NASH karakterizira prekomjerno nakupljanje masti u hepatocitima i inducirano oštećenje stanica i upala, sa ili bez hepatičke fibroze. Težina fibroze jetre kod pacijenata s NASH-om usko je povezana s lošom prognozom jetre (ciroza i njezine komplikacije te hepatocelularni karcinom), kardiovaskularnim događajima, ekstrahepatičnim malignim bolestima i smrću od svih uzroka. NASH može negativno utjecati na kvalitetu života pacijenata; međutim, nijedan lijek ili terapija nije odobrena za liječenje NASH-a.
Nedavna studija (ENLIVEN) objavljena u časopisu New England Journal of Medicine (NEJM) pokazala je da pegozafermin poboljšava i fibrozu jetre i upalu jetre kod pacijenata s NASH-om bez ciroze potvrđenom biopsijom.
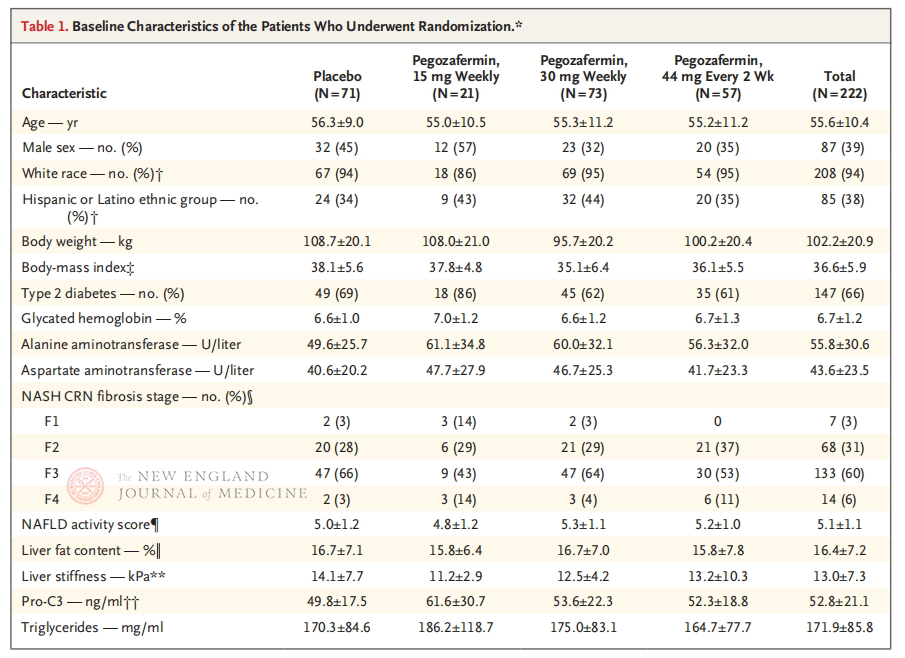
Multicentrično, randomizirano, dvostruko slijepo, placebom kontrolirano kliničko ispitivanje faze 2b, koje su proveli profesor Rohit Loomba i njegov klinički tim na Medicinskom fakultetu Sveučilišta Kalifornija u San Diegu, uključilo je 222 pacijenta s biopsijom potvrđenim NASH-om stadija F2-3 između 28. rujna 2021. i 15. kolovoza 2022. Nasumično su raspoređeni u skupine koje su primale pegozafermin (supkutana injekcija, 15 mg ili 30 mg jednom tjedno ili 44 mg jednom svaka 2 tjedna) ili placebo (jednom tjedno ili jednom svaka 2 tjedna). Primarni ishodi uključivali su poboljšanje fibroze ≥ stadija 1 i bez progresije NASH-a. NASH se povukao bez fibrotične progresije. Studija je također provela procjenu sigurnosti.
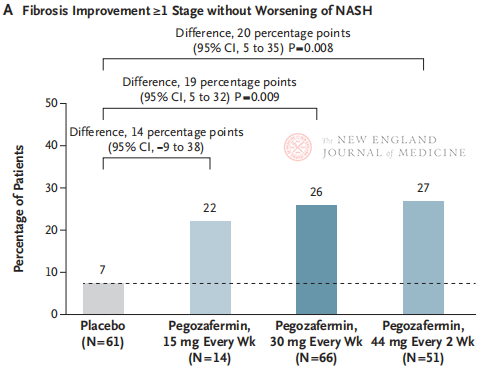
Nakon 24 tjedna liječenja, udio pacijenata s poboljšanjem fibroze ≥ stadija 1 i bez pogoršanja NASH-a, te udio pacijenata s regresijom NASH-a i bez pogoršanja fibroze bili su značajno veći u tri skupine koje su primale pegozafermin nego u skupini koja je primala placebo, sa značajnijim razlikama u pacijenata liječenih s 44 mg jednom svaka dva tjedna ili 30 mg jednom tjedno. Što se tiče sigurnosti, pegozafermin je bio sličan placebu. Najčešći štetni događaji povezani s liječenjem pegozaferminom bili su mučnina, proljev i eritem na mjestu injekcije. U ovom ispitivanju faze 2b, preliminarni rezultati sugeriraju da liječenje pegozaferminom poboljšava fibrozu jetre.
Pegozafermin, korišten u ovoj studiji, dugodjelujući je glikozilirani analog humanog faktora rasta fibroblasta 21 (FGF21). FGF21 je endogeni metabolički hormon koji luči jetra, a igra ulogu u regulaciji metabolizma lipida i glukoze. Prethodne studije pokazale su da FGF21 ima terapijske učinke na pacijente s NASH-om povećanjem osjetljivosti jetre na inzulin, stimuliranjem oksidacije masnih kiselina i inhibiranjem lipogeneze. Međutim, kratko vrijeme poluraspada prirodnog FGF21 (oko 2 sata) ograničava njegovu upotrebu u kliničkom liječenju NASH-a. Pegozafermin koristi tehnologiju glikozilirane pegilacije kako bi produžio vrijeme poluraspada prirodnog FGF21 i optimizirao njegovu biološku aktivnost.
Uz pozitivne rezultate u ovom kliničkom ispitivanju faze 2b, druga nedavna studija objavljena u časopisu Nature Medicine (ENTRIGUE) pokazala je da pegozafermin također značajno smanjuje trigliceride, ne-HDL kolesterol, apolipoprotein B i steatozu jetre u bolesnika s teškom hipertrigliceridemijom, što može imati pozitivan utjecaj na smanjenje rizika od kardiovaskularnih događaja u bolesnika s NASH-om.
Ove studije ukazuju na to da pegozafermin, kao endogeni metabolički hormon, može pružiti višestruke metaboličke koristi pacijentima s NASH-om, posebno zato što bi NASH u budućnosti mogao biti preimenovan u metabolički povezanu masnu bolest jetre. Ovi rezultati čine ga vrlo važnim potencijalnim lijekom za liječenje NASH-a. Istovremeno, ovi pozitivni rezultati studije podržat će uvođenje pegozafermina u klinička ispitivanja faze 3.
Iako je i dvotjedno liječenje pegozaferminom od 44 mg ili tjedno liječenje s 30 mg postiglo histološki primarni cilj ispitivanja, trajanje liječenja u ovoj studiji bilo je samo 24 tjedna, a stopa suradljivosti u placebo skupini bila je samo 7%, što je značajno niže od rezultata prethodnih kliničkih studija koje su trajale 48 tjedana. Jesu li razlike i sigurnost iste? S obzirom na heterogenost NASH-a, u budućnosti su potrebna veća, multicentrična, međunarodna klinička ispitivanja kako bi se uključile veće populacije pacijenata i produžilo trajanje liječenja radi bolje procjene učinkovitosti i sigurnosti lijeka.
Vrijeme objave: 16. rujna 2023.